すり込み理科ちゃん「再結晶」
はい、『すり込み理科ちゃん』今回は「再結晶」の巻。
先に覚えて欲しいキーワードを言っちゃうね。
再結晶
溶解度
飽和水溶液
ミョウバン
食塩=塩化ナトリウム
これだけ。
ちょっと多い?
じゃ、まずこれだけ。
溶解度
飽和水溶液
この2つ。
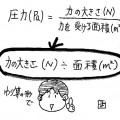
水100グラムに溶ける物質の最大の質量を溶解度という。
要するに、100グラムの水に何グラムまでその物質が溶けるのかっていう質量のこと。
これは温度によって変わる。
水より、お湯のほうがよく溶けるからね。
溶けるだけ目一杯溶かした状態の水溶液を、飽和水溶液という。
はい、すり込みすり込みー。
でもって、再結晶の話だけど。
物質を水に溶かして、その粒をまた取り出すのが再結晶。
方法は2つ。
① 温かいお湯に目一杯溶かして、ガーッと冷やす。
② 水溶液を加熱して、水を蒸発させる。
どっちがお好み?
代表例で覚えておこう。
ミョウバンは①
食塩(塩化ナトリウムともいう)は②
これを見てちょーだい。
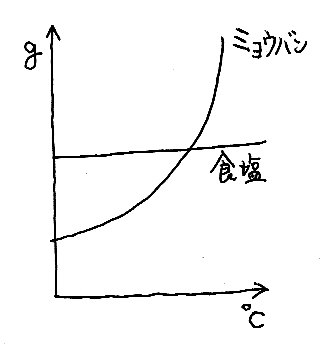
ミョウバンの溶解度は、温度が高くなるとグイーッと大きくなるね。
だから、熱いお湯と冷たい水では溶ける質量に差が出来るから、冷やせば溶け切れなくなった粒が出てくる。
食塩は水の温度が変わってもあまり溶解度の差がないから、冷やしてもそのまんま溶けてる。
で、粒は出てこないから、②の方法。
加熱して水を蒸発させて粒を取りだす。
はい、すり込みすり込みー。
最後に、これも覚えといて。
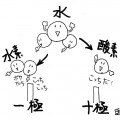
結晶の形。
この2つだけ。

はい、すり込みすり込みー。

このページに対してのコメント